鹽酸千金藤堿逆轉(zhuǎn)MCF-7/ADR細胞多藥耐藥性的作用及其機制
夏 薇,王 寧,王慶端
(河南省醫(yī)藥科學研究院藥化室,鄭州 450052)
鹽酸千金藤堿逆轉(zhuǎn)MCF-7/ADR細胞多藥耐藥性的作用及其機制
夏 薇,王 寧,王慶端△
(河南省醫(yī)藥科學研究院藥化室,鄭州 450052)
目的研究鹽酸千金藤堿(CH)對人乳腺上皮細胞癌耐藥細胞株MCF-7/阿霉素(ADR)多藥耐藥性的體外逆轉(zhuǎn)作用,并探討其逆轉(zhuǎn)機制?方法 用四甲基偶氮唑鹽(M TT)法檢測CH對多藥耐藥腫瘤細胞MCF-7/ADR的耐藥逆轉(zhuǎn)活性;免疫組織化學法檢測細胞內(nèi)谷胱甘肽硫轉(zhuǎn)移酶π(GST-π)的表達;通過對超螺旋PBR322 DNA的解旋能力檢測拓撲異構(gòu)酶Ⅱ(TopoⅡ)的活性?結(jié)果CH在無細胞毒濃度下具有逆轉(zhuǎn)MCF-7/ADR細胞耐藥性的作用,逆轉(zhuǎn)倍數(shù)為13.5倍,但對敏感株MCF-7細胞的抗癌藥物敏感性基本無影響?CH 4μ mol/L使MCF-7/ADR細胞中過度表達的GST-π的表達水平下降及DNA TopoⅡ的催化活性提高,但對敏感株MCF-7細胞無影響?結(jié)論CH具有逆轉(zhuǎn)多藥耐藥性的作用,其機制可能與降低GST-π的表達及提高DNA TopoⅡ的活性有關(guān)?
乳腺腫瘤;抗藥性,多藥;谷胱甘肽轉(zhuǎn)移酶;DNA拓撲異構(gòu)酶;鹽酸千金藤堿
腫瘤多藥耐藥性(multidrug resistance,M DR)是腫瘤化療失敗的主要原因,谷胱甘肽硫轉(zhuǎn)移酶π(glutathione S-transferase pi,GST-π)通過對異生物質(zhì)的生物轉(zhuǎn)化和解毒功能參與腫瘤細胞耐藥性的形成[1];而DNA拓撲異構(gòu)酶Ⅱ(topoisomeraseⅡ,TopoⅡ)活性數(shù)量或性質(zhì)上的改變引起藥物誘導產(chǎn)生的可裂解復合物的形成減少,從而導致MDR的產(chǎn)生[2]?鹽酸千金藤堿(cepharanthine hydrochloride,CH)是從防己科千金藤屬植物的塊根中提取分離出的一種雙芐基異喹啉類生物堿單體化合物,具有較強的多種生物活性[3],其分子式為C37H38N2O6?HCl,相對分子質(zhì)量為679.628,現(xiàn)國家食品藥品監(jiān)督管理局(SFDA)已批準進入Ⅱ期臨床研究(臨床批號:2005L00390)?有研究表明千金藤堿具有逆轉(zhuǎn)腫瘤MDR的作用[4]?但其機制是否與GST-π及DNA TopoⅡ有關(guān)的研究尚無報道?本研究旨在探討CH對人乳腺上皮細胞癌M DR細胞M CF-7/阿霉素(adriamycin,ADR)耐藥性的逆轉(zhuǎn)作用及其逆轉(zhuǎn)機制?
1 材料與方法
1.1 細胞株與細胞培養(yǎng) 人乳腺上皮細胞腺癌MCF-7細胞株及耐ADR細胞株MCF-7/ADR均引自中國科學院上海藥物研究所?兩細胞株培養(yǎng)于含體積分數(shù)10%胎牛血清,1×105U/L青霉素和100 mg/L鏈霉素的RPMI-1640完全培養(yǎng)基中,置于37℃?飽和濕度及5%CO2的細胞培養(yǎng)箱內(nèi)?細胞經(jīng)消化傳代,取對數(shù)生長期細胞進行培養(yǎng),MCF-7/ADR細胞傳代時在完全培養(yǎng)基中加入2 μ mol/L ADR以維持其MDR表型,實驗前無藥培養(yǎng)2周?
1.2 材料與儀器 CH為河南省醫(yī)藥科學研究院?中科院昆明植物研究所和廣州暨南大學共同研究并提供,經(jīng)檢測達質(zhì)譜純?ADR為意大利Farmitalia公司產(chǎn)品,RPMI-1640培養(yǎng)基為美國Gibco產(chǎn)品,四甲基偶氮唑鹽(M TT)為瑞士Fluka公司產(chǎn)品,兔抗人GST-π多克隆抗體?SP免疫組化染色試劑盒?DAB試劑盒購自北京中杉金橋生物技術(shù)有限公司,pBR322DNA為華美生物工程公司產(chǎn)品?DNA expert自動酶聯(lián)免疫檢測儀為奧地利Tecan公司產(chǎn)品,HPIAS-1000彩色病理圖文分析系統(tǒng)為同濟醫(yī)科大學千屏影像工程公司提供,Gene Genius凝膠圖像分析系統(tǒng)為英國Syugene公司產(chǎn)品?
1.3 M TT法測定藥物的細胞毒作用[5]取對數(shù)生長期MCF-7?M CF-7/ADR細胞,制成細胞濃度8×107個/L的細胞懸液,接種于96孔細胞培養(yǎng)板,每孔100μL,培養(yǎng)24 h待細胞貼壁后,更換培養(yǎng)液,加入不同濃度的ADR?CH或維拉帕米(Verapamil,VER),每孔終體積為200 μ L,每組4個平行孔,細胞與藥物作用72 h后每孔加入M TT溶液(5 g/L)20μ L,繼續(xù)培養(yǎng)4 h,棄去孔內(nèi)培養(yǎng)液,加入二甲亞砜(DMSO)150 μ L/孔,用微量振蕩器振蕩10 min,完全溶解后用酶聯(lián)免疫檢測儀在570 nm波長處測定吸光度值(A值)?計算抑制率?半數(shù)抑制濃度(IC50)?耐藥倍數(shù)(耐藥株 IC50/敏感株 IC50)?逆轉(zhuǎn)倍數(shù)(耐藥株IC50/加逆轉(zhuǎn)劑后耐藥株IC50)等?
1.4 細胞內(nèi)GST-π表達的測定[6]運用免疫組化第二代LAB-SA檢測技術(shù)測定GST-π的表達,并加以改進?處理蓋玻片制備細胞爬片,取對數(shù)生長期細胞 MCF-7?MCF-7/ADR,以細胞數(shù)5×108個/L植入放有蓋玻片的 24孔培養(yǎng)板,每孔 1 mL,培養(yǎng)24 h后,更換為含有不同濃度藥物的培養(yǎng)液,繼續(xù)培養(yǎng)12 h,取出蓋玻片,用 PBS(0.01 M?pH7.4)液洗滌2次,4℃丙酮固定10 min,PBS洗滌3次后,按試劑盒說明書操作,一抗為1∶100兔抗人GST-π多克隆抗體,PBS代替一抗作為陰性對照?采用HPIAS-1000型彩色病理圖文分析系統(tǒng)進行圖像分析,于400倍顯微鏡下各測定7個視域細胞中GST-π的含量,以細胞積分光密度值對結(jié)果進行評價?
1.5 DNA TopoⅡ活性的測定 細胞培養(yǎng)及藥物處理分組同前,經(jīng)不同濃度藥物作用24 h后,收集 MCF-7?MCF-7/ADR細胞各5×107個,按照文獻[7]的方法,加以改進提取拓撲異構(gòu)酶?采用考馬斯亮藍法定量測定酶提取液的蛋白含量?按照文獻[8]的方法,以pBR322DNA為底物觀察耐藥株及敏感株細胞DNA TopoⅡ?qū)BR322DNA的解旋能力及藥物對其影響?將瓊脂糖凝膠電泳結(jié)果用Gene Genius凝膠圖相分析系統(tǒng)照相并對超螺旋DNA條帶進行半定量分析,以加酶組與空白對照組的吸光度比值作為DNA TopoⅡ活性量化指標?
1.6 統(tǒng)計學處理 采用SPSS10.0統(tǒng)計軟件分析,實驗數(shù)據(jù)以±s表示,各參數(shù)多個樣本均數(shù)比較用單因素方差分析,兩樣本均數(shù)比較用t檢驗,進行統(tǒng)計學處理?
2 結(jié) 果
2.1 多藥耐藥細胞株MCF-7/ADR的耐藥性測定 ADR對
MCF-7/ADR及MCF-7細胞的IC50值分別為(27.37±0.83)?(0.50±0.03)μ mol/L?耐藥倍數(shù)為54.7倍?
2.2 CH體外逆轉(zhuǎn)耐藥性的作用 CH在體外對MCF-7及MCF-7/ADR細胞毒作用較弱,8 μ mol/L CH的抑制率分別為(9.86±2.03)%?(10.27±1.25)%,4 μ mol/L CH 時分別為(4.75±0.58)%?(5.10 ±0.82)%,2 μ mol/L CH 時分別為(2.15±0.47)%?(2.34±0.71)%,在逆轉(zhuǎn)耐藥性所用的濃度下,基本不影響細胞存活率?CH可部分增加MCF-7/ADR對ADR的敏感性,對敏感株 MCF-7細胞無影響?4 μ mol/L CH對M CF-7/ADR細胞耐藥性的逆轉(zhuǎn)倍數(shù)為 13.5倍,而 8 μ mol/L VER的逆轉(zhuǎn)倍數(shù)為7.3倍,CH對MCF-7/ADR的逆轉(zhuǎn)活性強于 VER(P0.05),見表1?
2.3 CH對MCF-7/ADR細胞質(zhì)GST-π表達的影響 MCF-7及M CF-7/ADR細胞中 GST-π均有表達,但 MCF-7/ADR細胞中GST-π呈高表達,而 MCF-7細胞中GST-π呈較低表達,兩者相比差異有統(tǒng)計學意義(P0.05)?單用0.17 μ mol/L ADR處理MCF-7細胞及單用 9.12 μ mol/L ADR處理MCF-7/ADR細胞均不影響 GST-π 表達,與 4 μ mol/L CH 合用后可降低 MCF-7/ADR細胞中GST-π的表達水平(P0.05),但未下降至敏感細胞水平,而對MCF-7細胞無影響?與8 μ mol/L VER合用后也降低 MCF-7/ADR細胞中 GST-π的表達水平,但作用弱于CH,對敏感細胞無影響,見表2?
表1 CH對MCF-7及MCF-7/ADR敏感性的影響(±s,n=12)
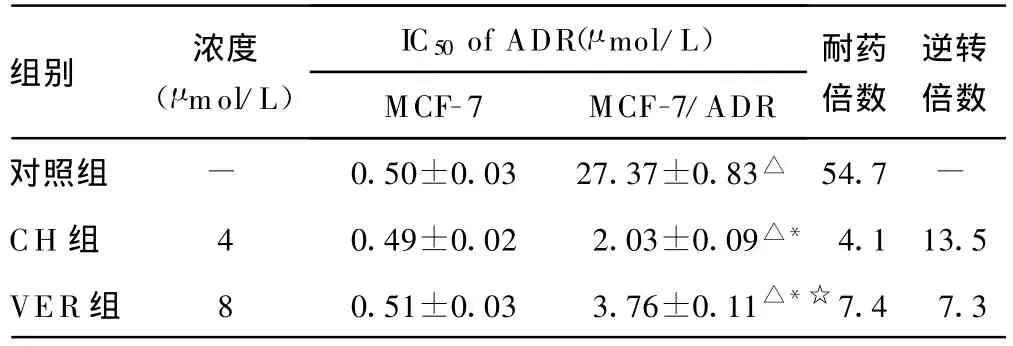
表1 CH對MCF-7及MCF-7/ADR敏感性的影響(±s,n=12)
△:P0.05,與同組 MCF-7比較;*:P0.05,與對照組MCF-7/ADR比較;☆:P0.05,與CH 組MCF-7/ADR比較;-:表示無數(shù)據(jù)?
組別 濃度(μ mol/L)IC50of ADR(μ mol/L)MCF-7 MCF-7/ADR耐藥倍數(shù)逆轉(zhuǎn)倍數(shù)對照組 - 0.50±0.03 27.37±0.83△ 54.7 -CH 組 4 0.49±0.02 2.03±0.09△* 4.113.5 VER組 8 0.51±0.03 3.76±0.11△*☆7.4 7.3
表2 CH對 MCF-7及MCF-7/ADR細胞中GST-π表達的影響(±s,n=7)
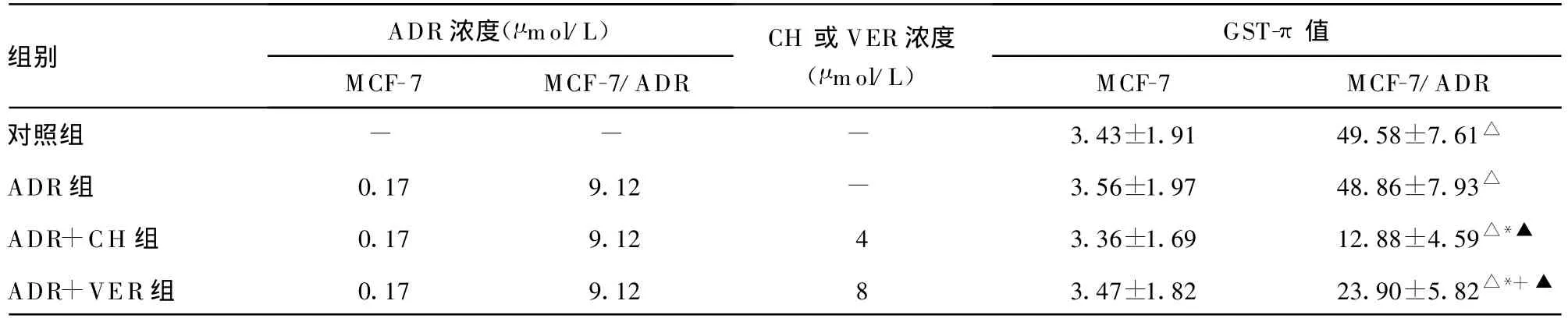
表2 CH對 MCF-7及MCF-7/ADR細胞中GST-π表達的影響(±s,n=7)
△:P0.05,與同組MCF-7比較;*:P0.05,與對照組MCF-7/ADR比較;+:P0.05,與ADR+CH 組MCF-7/ADR組比較;▲:P0.05,與ADR組MCF-7/ADR比較;-:表示無數(shù)據(jù)?
組別ADR 濃度(μ mol/L)MCF-7 MCF-7/ADR CH或VER濃度(μ mol/L)GST-π值MCF-7 MCF-7/ADR對照組 - - - 3.43±1.91 49.58±7.61△ADR組 0.17 9.12 - 3.56±1.97 48.86±7.93△ADR+CH 組 0.17 9.12 4 3.36±1.69 12.88±4.59△*▲ADR+VER組 0.17 9.12 8 3.47±1.82 23.90±5.82△*+▲
表3 CH對MCF-7及MCF-7/ADR細胞DNA TopoⅡ催化活性的影響(±s,n=10)
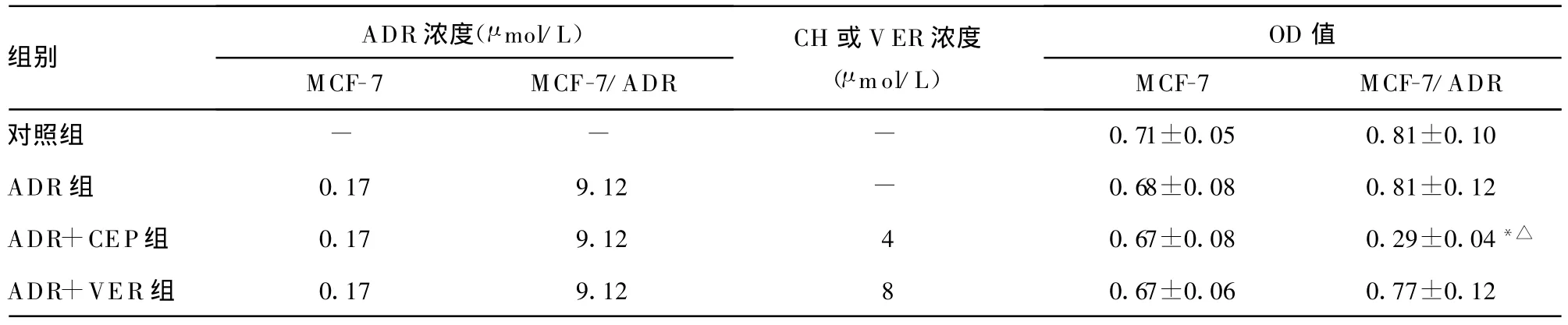
表3 CH對MCF-7及MCF-7/ADR細胞DNA TopoⅡ催化活性的影響(±s,n=10)
*:P0.05,與對照組MCF-7/ADR比較;△:P0.05,與ADR組MCF-7/ADR組比較;-:表示無數(shù)據(jù)?
組別 ADR濃度(μ mol/L)MCF-7 MCF-7/ADR CH或V ER濃度(μ mol/L)OD值MCF-7 MCF-7/ADR對照組 - - - 0.71±0.05 0.81±0.10 ADR組 0.17 9.12 - 0.68±0.08 0.81±0.12 ADR+CEP組 0.17 9.12 4 0.67±0.08 0.29±0.04*△ADR+VER組 0.17 9.12 8 0.67±0.06 0.77±0.12
2.4 CH對MCF-7/ADR細胞核內(nèi)DNA TopoⅡ催化活性的影響 DNA TopoⅡ催化活性測定結(jié)果表明,單用0.17 μ mol/L ADR處理 MCF-7細胞及單用9.12 μ mol/L ADR處理MCF-7/ADR細胞,與加酶無藥對照組相比差異均無統(tǒng)計學意義(P>0.05)?與4 μ mol/L CH 合用可促進MCF-7/ADR細胞DNA TopoⅡ介導的 DNA解旋作用,而對MCF-7細胞無影響?與8 μ mol/L VER合用對MCF-7及MCF-7/ADR細胞DNA TopoⅡ活性均無影響,見表3?圖1?根據(jù)1個酶活性單位所需蛋白含量,MCF-7/ADR細胞為 MCF-7細胞的2.4倍,蛋白含量分別為(2.93±0.25)μ g和(1.22±0.16)μ g?
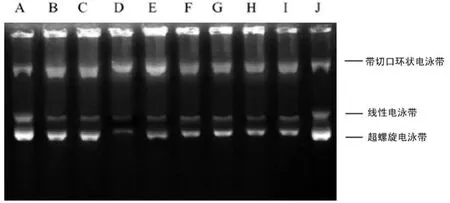
圖 1 MCF-7及MCF-7/ADR細胞DNA TopoⅡ催化活性
3 討 論
腫瘤M DR的發(fā)生存在多機制?多途徑?多環(huán)節(jié),在抗腫瘤藥物殺傷腫瘤細胞的通道上發(fā)生任何改變均可導致抗藥性的產(chǎn)生,涉及抗癌藥物的轉(zhuǎn)運?代謝和抗癌藥物作用靶點,細胞識別毒性損傷,細胞損傷修復機制以及細胞凋亡等[9]?近年來研究顯示以胞漿中谷胱甘肽硫轉(zhuǎn)移酶(GSTs)介導的MDR和以細胞核內(nèi)酶TopoⅡ介導的非經(jīng)典耐藥途徑(AT-MDR),在MDR的發(fā)生過程中發(fā)揮重要作用[10-11]?
本實驗所用的MCF-7/ADR細胞由對人乳腺癌細胞MCF-7經(jīng)遞增濃度的ADR反復誘導篩選獲得的具典型MDR表型的細胞株?通過對兩細胞株活性的測定,MCF-7/ADR細胞相對于親代敏感細胞MCF-7耐藥倍數(shù)為54.7倍?體外逆轉(zhuǎn)活性表明CH對MCF-7/ADR的耐藥性有明顯的逆轉(zhuǎn)作用?在非細胞毒劑量下的CH?VER可增加MCF-7/ADR細胞對 ADR的敏感性,4 μ mol/L CH的逆轉(zhuǎn)倍數(shù)為 13.5,8 μ mol/L VER的逆轉(zhuǎn)倍數(shù)為7.3,CH的逆轉(zhuǎn)作用強于VER?
GSTs是一組具有多種生理功能的同工酶蛋白,對異生物質(zhì)的生物轉(zhuǎn)化和解毒具有重要作用,主要存在于細胞質(zhì)中?GST-π基因表達受多水平調(diào)控,在多種耐藥性腫瘤細胞株中過量表達,與腫瘤細胞的耐藥性密切相關(guān)[12]?GST-π可催化GSH的巰基與親電性抗腫瘤藥物結(jié)合,消除原來的活性親電部位,增加藥物在水中的溶解度,降低其化學反應(yīng),水溶性谷胱甘肽-S-化合物經(jīng)巰基尿酸生物合成途徑代謝,加速抗腫瘤藥物的降解,使藥物在靶部位的積蓄量迅速減少而達不到致死濃度,導致腫瘤MDR的產(chǎn)生[13]?
DNA TopoⅡ是催化DNA拓撲結(jié)構(gòu)改變的酶,為核基質(zhì)成分之一,是腫瘤化療的重要靶酶,與多種抗癌藥物的細胞毒效應(yīng)有關(guān)[14]?細胞對抗腫瘤藥物的敏感性依賴于靶酶的水平,通過對分離出的抗藥細胞核仁和核基質(zhì)的研究證實,藥物敏感性的降低在于藥物誘導產(chǎn)生的可裂解復合物的形成減少;藥物引起的DNA斷裂減少和抗藥細胞毒性的降低為抗藥細胞內(nèi)TopoⅡ活性降低所致?TopoⅡ介導的at-MDR的生化基礎(chǔ)在于TopoⅡ活性數(shù)量或性質(zhì)上的改變[15]?(2):167-177.
本實驗結(jié)果顯示,MCF-7/ADR細胞GST-π高表達,為MCF-7細胞的14.5倍,進一步證實GST-π高表達可導致MDR產(chǎn)生;而MCF-7/ADR細胞1個酶活性單位所需的蛋白含量為MCF-7細胞的2.4倍,DNA TopoⅡ的活性明顯降低,說明腫瘤細胞耐藥性在一定程度上與TopoⅡ的含量和活性的下降有關(guān),與國外研究結(jié)果一致[16]?CH?VER均可降低MCF-7/ADR細胞GST-π的表達,CH可提高DNA TopoⅡ的活性,而對敏感株MCF-7無明顯影響,表明CH逆轉(zhuǎn)M DR的機制可能與降低GST-π的表達及增加DNA TopoⅡ的活性有關(guān)?有研究表明,在乳腺癌中 GST-π與 MDR相關(guān)蛋白(MRP)?mdr1存在共表達,而共表達是耐藥相關(guān)標志受共同因子調(diào)控的證據(jù)[17],因此,VER能有效逆轉(zhuǎn)P-gp介導的耐藥,部分逆轉(zhuǎn) MRP介導的耐藥,可能是其在一定程度上降低GST-π表達的機制,但與 TopoⅡ介導的 at-MDR途徑無關(guān)?
GST-π的表達及TopoⅡ介導的at-MDR途徑,受多水平調(diào)控,作用通路具有復雜性,CH通過何種機制影響GST-π的表達及TopoⅡ的活性,有待進一步研究?CH是從防己科千金藤屬植物提取出來的生物堿單體化合物,日本已用于治療臨床放?化療所致的白細胞減少20余年,大劑量用藥而未發(fā)現(xiàn)明顯毒副作用,對該藥進一步研究并作為腫瘤化療的耐藥逆轉(zhuǎn)劑應(yīng)用于臨床提供了重要依據(jù)?
[1] Teodori E,Dei S,Scapecchi S,et al.The medicinal chemistry of multidrug resistance(M DR)reversing drugs[J].Farmaco,2002,57(5):385-415.
[2] Liem AA,Chamberlain M P,Wolf CR,et al.The role of signal transduction in cancer treatment and drug resistance[J].Eur J Surg Oncol,2002,28(6):679-684.
[3] 王金華,葉祖光,孫愛續(xù),等.粉防己堿逆轉(zhuǎn)耐阿霉素的人乳腺癌MCF-7細胞的抗凋亡作用[J].中國組織化學與細胞化學雜志,2000,9(4):436-440.
[4] 宋玉成,夏薇,江金花,等.鹽酸千金藤素逆轉(zhuǎn) EAC/ADR細胞多藥耐藥性的作用及其機制[J].藥學學報,2005,40(3):204-207.
[5] 郭偉劍,李杰,沈兆忠,等.外源性 TNF-a基因聯(lián)合異博定?三苯氧胺逆轉(zhuǎn)多藥耐藥性[J].復旦學報:醫(yī)學版,2001,28(2):141-144.
[6] 辛華.細胞生物學實驗[M].北京:科學出版社,2001:81-86.
[7] Markovits J,Larsen AK,Segal-Bendirdjian E,et al.Inhibition of DNA topoisomerases I andⅡand induction of apoptosis by erbstatin and tyrphostin derviatives[J].Biochem Pharmacol,1994,48:549-560.
[8] Marx G,Zhou H,David E,et al.Covalent attachment of ethidium to DNA Results in enhanced topoisomeraseⅡ-mediated DNA cleavage[J].Biochemistry,1997,36:15884-15891.
[9] 李偉,胡凱文.腫瘤多藥耐藥研究現(xiàn)狀[J].中國中醫(yī)藥信息雜志,2000,7(7):68.
[10]Bernardini S,Bellincampi L,Ballerini S,et al.Role of GST P1-1 in mediating the effect of etoposide on human neuroblastoma cell line Sh-Sy5y[J].J Cell Biochem,2002,86(2):340-347.
[11]Goekkurt E,Hoehn S,Wolschke C,et al.Polymorphisms of glutathione S-transferases(GST)and thymidylate synthase(TS)-novel predictors for response and survival in gastric cancer patients[J].Br J Cancer,2006,94:281-286.
[12]王秀麗,孔力,趙瑾瑤,等.三氧化二砷逆轉(zhuǎn)人乳腺癌MCF-7/ADM細胞耐藥的機制研究[J].中華腫瘤雜志,2002,24(4):339-343.
[13]Ichihara T,Wanibuchi H,Taniyama T,et al.Inhibition of liver glut athione S-transferase placental form positive foci development in the rat hepatocarcino-genesis by Porphyra tenera(Asakusa-nori)[J].Cancer Lett,1999,141:211-218.
[14] Tanner B,Pilch H,Schaffer U,et al.Expression of C-erbB-2 and topoisomeraseⅡ alpha in rdlation to chemoresistance in ovarian cancer[J].Zentralbl Gynakol,2002,124(3):176-183.
[15]Korkolopoulou P,Angelopoulou M,Siakantari M,et al.Evalution of DNA topoisomeraseⅡa expression provides independent prognostic information in non-Hodgkin′s lymphomas[J].Histopathology,2001,38:45-53.
[16]Scheltema JMW,Romijn JC,Van Steenbragge GJ,et al.Inhibition of apoptotic proteins causes multidrug resistance in renal carcinoma cells[J].Anticancer Res,2001,21(5):3161-3166.
[17]Kreisholt J,Sorensen M,Jensen PB,et al.Immunohistochemical detection of DNA topoisomeraseⅡalpha P-glycoprotein and multidrugresistance protein(M RP)in small-cell and non-small-cell lung cancer[J].Br J Cancer,1998,77:1469-1473.
Reversal of multidrug resistance in MCF-7/ADR cells by cepharanthine hydrochloride and its mechanism
ObjectiveTo investigate the reversal effect of cepharanthine hydrochloride(CH)on multidrug resistance(MDR)of drug-resistant cell line of human breast epithelial carcimoma(MCF-7/ADR),and to explore its mechanism.MethodsM TT assay was used to detect cytotoxicity and MDR reversal activity of CH in MCF-7/ADR cell line.Immunohistochemistry(IHC)technique was used to show the intracellular expression of glutathione S-transferases pi(GST-π).The catalytic activity of DNA Topoisomerase(TopoⅡ)was assessed by the ATP-dependent relaxation of supercoild pBR322 DNA.ResultsCH could enhance sensitivity of MCF-7/ADR cells to anti-tumor drugs.A 13.5 fold reversed effect of resistance was achieved in vitro.However,CH had few effects on drug-sensitive MCF-7 cells.After treatment of CH under the concentration of 4μ mol/L,the level of higher expression of GST-π was decreased and the activity of DNA TopoⅡwas increased in MCF-7/ADR cell line,but no changes was found in MCF-7 cells.ConclusionCH is able to effectively reverse drug resistance and its mechanism is probably related to reducing the expression of GST-πand enhancing the activity of DNA TopoⅡ in MDR tumor cells.
breast neoplasms;drug resistance,multiple;glutathione transferase;DNA topoisomerase;cepharanthine hydrochloride
10.3969/j.issn.1671-8348.2011.01.006
A
1671-8348(2011)01-0014-03
△通訊作,電話:(0371)66658216;E-mail:wangningxiao3@126.com?
2010-03-10
2010-06-23)
?論 著?

